Thema im Fokus
Standards und Praxis der Embryonenforschung
Foto: Adobe Stock / sinitar
Auf internationaler Ebene existieren keine verbindlichen Abkommen über die Forschung mit humanen Embryonen. In zahlreichen Ländern ist diese in engen Grenzen erlaubt. In der Regel darf nur bis zu 14 Tage nach der Befruchtung an Embryonen außerhalb des menschlichen Körpers geforscht werden. Forschenden gelingt es inzwischen auch, embryoähnliche Zellformationen aus Stammzellen zu erzeugen.
Internationale und nationale Regeln
Weder auf Ebene der Vereinten Nationen noch auf europäischer Ebene existieren einheitliche Regelungen zur Forschung mit humanen Embryonen beziehungsweise mit den aus ihnen gewonnenen humanen embryonalen Stammzellen (hES-Zellen). Zugleich gibt es eine Reihe von Stellungnahmen und Regulierungsansätzen, die für die Durchführbarkeit und mögliche Ziele der Forschung mit humanen Embryonen relevant sind.
„Das Embryonenschutzgesetz setzt den wenige Tage alten Embryo in Menschenwürde und Lebensschutz einem geborenen Menschen gleich.“
In Deutschland verbietet das 1990 verabschiedete Embryonenschutzgesetz (ESchG) die Forschung mit frühen menschlichen Embryonen außerhalb des Körpers. Wissenschaftlerinnen und Wissenschaftler können hierzulande daher wenig zur Aufklärung wichtiger Forschungsfragen der frühen menschlichen Entwicklungsbiologie beitragen. Dasselbe Gesetz untersagt zudem die Gewinnung von Stammzellen aus menschlichen Embryonen (hES-Zellen). Das deutsche Stammzellgesetz (StZG) hingegen erlaubt – unter bestimmten Voraussetzungen – den Import von im Ausland erzeugten embryonalen Stammzellen und deren Verwendung für hochrangige Forschungsziele.
„In Deutschland profitieren wir von embryonalen Stammzellen, die im Ausland generiert wurden.“
In Ländern wie den USA, Israel, Schweden, Großbritannien, Frankreich oder Japan ist die In-vitro-Forschung an frühen menschlichen Embryonen in engen Grenzen erlaubt. Die Forschung darf dort an sogenannten überzähligen Embryonen für 14 Tage nach der Befruchtung erfolgen, anschließend müssen die Embryonen verworfen werden. Überzählige Embryonen sind solche, die ursprünglich im Rahmen einer künstlichen Befruchtung erzeugt wurden, aber hierfür nicht mehr verwendet werden. In einigen dieser Länder ist auch die Erzeugung von Embryonen für die Forschung aus speziell für diesen Zweck gespendeten Keimzellen möglich. In der Regel muss begründet werden, warum die verfügbaren überzähligen Embryonen nicht ausreichen oder für das jeweilige Forschungsvorhaben ungeeignet sind.
Die Frist von 14 Tagen als Grenzlinie für die In-vitro-Forschung an Embryonen geht auf die bioethischen Empfehlungen des Warnock-Reports von 1984 zurück, der unter der Leitung der britischen Philosophin Mary Warnock erarbeitet wurde. Da es vor der Einnistung in der Gebärmutter auch bei natürlicher Befruchtung zu einem häufigen Absterben früher Embryonen kommt und da dieser der Zeitpunkt den eigentlichen Beginn der Schwangerschaft ausmacht, fand der Vorschlag damals internationale Akzeptanz. Zudem konnten In-vitro-Embryonen lange Zeit ohnehin nicht länger als fünf bis sechs Tage im Labor kultiviert werden. Da es zunehmend möglich ist die In-vitro-Embryonen über 14 Tage hinaus zu kultivieren, wird international eine Verlängerung der Frist etwa auf 28 Tage diskutiert, um Ursachen spontaner Schwangerschaftsverluste oder Erkrankungen, wie angeborene Herzfehler und Störungen des zentralen Nervensystems, besser erforschen und Therapien entwickeln zu können. Die Befürworter argumentieren, dass die Voraussetzungen für jegliche Empfindungsfähigkeit des Embryos bis zu diesem Zeitpunkt fehlten, da noch keinerlei funktionale Nervenverbindungen oder sensorische Systeme vorhanden sind.
Einige Forschungsfragen können nur mit Embryonen, die gezielt aus gespendeten Samen- und Eizellen für Forschungszwecke erzeugt wurden, beantwortet werden. Hier ist der experimentelle Ansatz direkt an den Befruchtungsprozess gekoppelt. Bei gespendeten überzähligen Embryonen sind dagegen bestimmte Prozesse bereits abgeschlossen, wie die Befruchtung selbst, die Bildung und Wanderung der Vorkerne sowie die Replikation der elterlichen Genome in den Vorkernen.
Alternative Verfahren der Stammzellforschung
Viele Erkenntnisse zur Embryonalentwicklung wurden bisher nur aus Tierversuchen, meist mit Mäusen, abgeleitet. Verlässliche Ergebnisse zur Entwicklung menschlichen Lebens, epigenetischer, genetischer und umweltbedingter Ursachen von Erkrankungen sowie die gezielte Entwicklung entsprechender Therapien können jedoch nicht allein aus Tiermodellen gewonnen werden. Es hat sich gezeigt, dass viele spezifische biologische Prozesse im Menschen anders ablaufen, beispielsweise die Befruchtung der Eizelle, die Zellteilung oder der Zeitpunkt der Aktivierung und Regulierung bestimmter Gene.
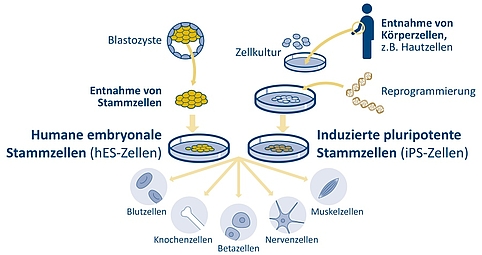
Eine potentielle Alternative zur Gewinnung von humanen embryonalen Stammzellen (hES-Zellen) stellen induzierte pluripotente Stammzellen (iPS-Zellen) dar. Forschenden ist es vor rund 15 Jahren erstmals gelungen, Körperzellen, die in ihrer Funktion bereits ausdifferenziert sind, zu pluripotenten Stammzellen umzuwandeln. Die iPS-Zellen können durch Reprogrammierung etwa aus adulten Haut- oder Blutzellen von Spenderinnen und Spendern gewonnen werden. Allerdings gibt es Hinweise darauf, dass iPS-Zellen genetische und epigenetische Unterschiede zu hES-Zellen aufweisen: Sie können zum einen epigenetische Muster der adulten Zellen, aus denen sie gewonnen wurden, übernehmen. Diese Unterschiede und die Frage, inwieweit die Differenzierung von hES- und iPS-Zellen in vitro der Embryonalentwicklung in vivo entspricht, sind Gegenstand der Embryonenforschung. Zum anderen werden Mutationen, die sich in den adulten Ursprungszellen im Laufe der Lebenszeit angesammelt haben, an die iPS-Zellen weitergegeben. Um solche Prozesse besser zu verstehen, müssten die iPS-Zellen mit den entsprechenden Stammzellen im Zellverband des Embryos sowie mit hES-Zellen verglichen werden. Solche Untersuchungen könnten auch über das Potential von iPS- und hES-Zellen für die Erforschung von Krankheiten sowie die Entwicklung von Zelltherapien Aufschluss geben.
Abbildung 2: Die Zellmasse im Inneren der Blastozyste enthält humane embryonale Stammzellen (hES). Diese lassen sich entnehmen und in vitro kultivieren. Sie sind pluripotent. Das bedeutet, sie besitzen die Fähigkeit, sich je nach Kulturbedingung in organspezifische Zelltypen zu differenzieren, beispielsweise in verschiedene Arten von Blut-, Knochen-, Nerven- oder Muskelzellen sowie insulinproduzierende Betazellen. Vor einigen Jahren fanden Forschende heraus, wie mittels genetischer Reprogrammierung aus adulten menschlichen Haut- oder Blutzellen sogenannte induzierte pluripotente Stammzellen (iPS-Zellen) erzeugt werden können. | Gestaltung: Emde Grafik
Der wissenschaftliche Fortschritt hat in den vergangenen Jahren dazu geführt, dass die Grenzen zwischen Körperzellen, Keimzellen und Embryonen zunehmend verschwimmen. Inzwischen wurden in der internationalen Stammzellforschung viele unterschiedliche Zellformationen (Embryoide) mit embryoähnlichen Eigenschaften erzeugt. So gelang es, aus iPS-Zellen verschiedene embryoähnliche Strukturen zu erzeugen, wie zum Beispiel blastulaähnliche Gebilde (Blastoide). Im Jahr 2023 konnten zudem erstmals weiter fortgeschrittene Entwicklungsstadien aus humanen embryonalen Stammzellen (hES-Zellen) gewonnen werden, ohne dass ein Befruchtungsprozess stattfand. Diese Stadien entsprechen normalerweise jenen, die sich kurz nach der Einnistung des Embryos in die Gebärmutter entwickeln. Das weitere Entwicklungspotential dieser Zellformationen ist noch offen – insbesondere, weil deren Entwicklung in vitro nach wenigen Tagen von selbst endet und es ethisch nicht vertretbar wäre, sie einem menschlichen Organismus einzupflanzen. Auch hier kann die vergleichende Embryonenforschung Aufschluss geben.
Veröffentlicht: Mai 2021, aktualisiert November 2023